Điện li là gì? Nguyên nhân dẫn đến ion hóa
Điện li là gì?
Điện li hay ion hoá là quá trình một nguyên tử hay phân tử tích một điện tích âm hay dương bằng cách nhận thêm hay mất đi electron để tạo thành các ion, thường đi kèm các thay đổi hoá học khác.[1] Ion dương được tạo thành khi chúng hấp thụ đủ năng lượng (năng lượng này phải lớn hơn hoặc bằng thế năng tương tác của electron trong nguyên tử) để giải phóng electron, những electron được giải phóng này được gọi là những electron tự do. Năng lượng cần thiết để xảy ra quá trình này gọi là năng lượng ion hoá.
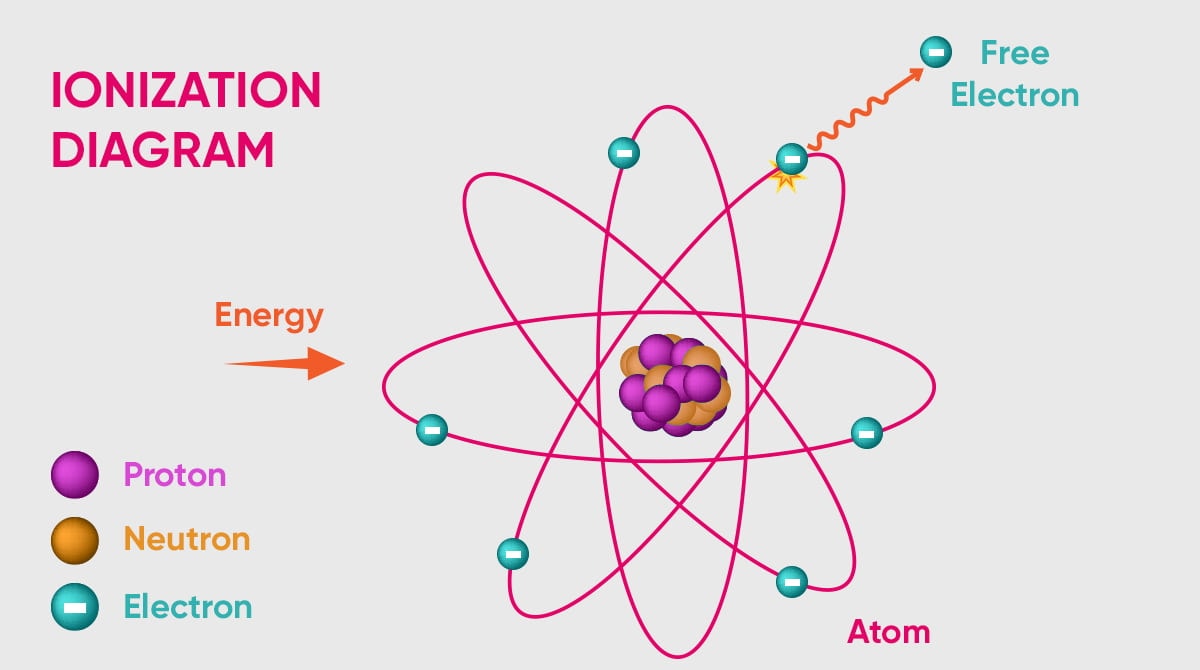
Nguyên nhân dẫn đến hiện tượng điện li
Phân tử nước bị phân cực thành hai đầu âm và dương do nguyên tử oxi có độ âm điện lớn hơn nguyên tử hiđro, cặp electron dùng chung bị lệch về phía oxi.
Độ điện li
Độ điện li α là tỉ số giữa số phân tử phân li ra ion (n) và tổng số phân tử hoà tan vào dung dịch (n0)
Độ điện li của các chất điện li khác nhau nằm trong khoảng 0 < α ≤ 1. Khi một chất, có α = 0, quá trình điện li không xảy ra, đó là chất không điện li. Độ điện li thường được biểu diễn dưới dạng phần trăm.
Chất điện li mạnh
Là chất khi tan trong nước và các phân tử hoà tan đều phân li ra ion. Các chất điện li mạnh có α = 1.
- Các bazơ mạnh: KOH, NaOH, Ca(OH)2, Ba(OH)2, …
- Các axit mạnh: HNO3, HCl, HI, HBr, H2SO4, HClO4, …
Tính tan của muối
- Muối của axit mạnh (HCl, H2SO4, HNO3, …):
- Muối clorua tan hết, trừ AgCl↓, PbCl2 ít tan.
- Muối sunfat tan hết, trừ PbSO4↓, CaSO4↓, SrSO4↓, BaSO4↓ và Ag2SO4 ít tan.
- Muối nitrat tan hết.
- Muối của axit yếu (H3PO4, H2SO3, …):
- Muối của natri, kali và muối axetat tan hết. Còn lại hầu hết tan.
- Muối axit (chứa H linh động trong phân tử): Hầu hết đều tan.
Phương trình điện li:
- Axit mạnh → Cation H+ + Anion gốc axit.
- Bazơ mạnh → Cation kim loại + Anion OH-.
- Muối tan → Cation kim loại/NH4+ + Anion gốc axit.
Chất điện li yếu
Là chất khi tan trong nước chỉ có một phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Axit yếu: HClO, H2S, HF, H2SO3, CH3COOH, H2CO3, …
- Bazơ yếu: Bi(OH)3, Mg(OH)2, Cu(OH)2, …
- Một số muối: HgCl2, Hg(CN)2, CuCl, …
Phân li – sự khác biệt
Một chất có thể phân li mà không nhất thiết tạo ra ion.
-
Ví dụ, các phân tử đường ăn (sucrose) phân ly trong nước (đường tan) nhưng vẫn tồn tại dưới dạng các phân tử trung hòa nguyên vẹn.
Một trường hợp tinh tế khác là phân li của natri clorua (muối ăn) thành các ion natri và clo. Mặc dù có vẻ như đây là một trường hợp ion hóa, thực tế các ion đã tồn tại sẵn trong mạng tinh thể. Khi muối phân li, các ion thành phần chỉ đơn giản được bao quanh bởi các phân tử nước và các tác dụng của chúng trở nên có thể quan sát (ví dụ: dung dịch dẫn điện). Tuy nhiên, không có sự chuyển giao hay dịch chuyển electron nào xảy ra.














